「新型コロナウイルス感染症にイベルメクチンが効果を発揮する」
このような言説が、一部で繰り返し発信されている。しかし、アメリカのFDA(食品医薬品局)やヨーロッパのEMA(欧州医薬品庁)はイベルメクチンを新型コロナ治療や予防に使うことに否定的だ。
何が「確か」と言えるのか。
BuzzFeed Newsは国立国際医療研究センターの国際感染症センタートラベルクリニック医長で予防接種支援センター長の氏家無限医師に話を聞いた。
(1)現段階ではイベルメクチンの効果を検証する質の高い臨床研究は十分ではない
(2)日本における薬の特例承認の基準を満たしていない
こうした点から、現時点でイベルメクチンは治療や予防に広く使用されるべきではないと考えられている。
現時点で「確か」と言えることとは?
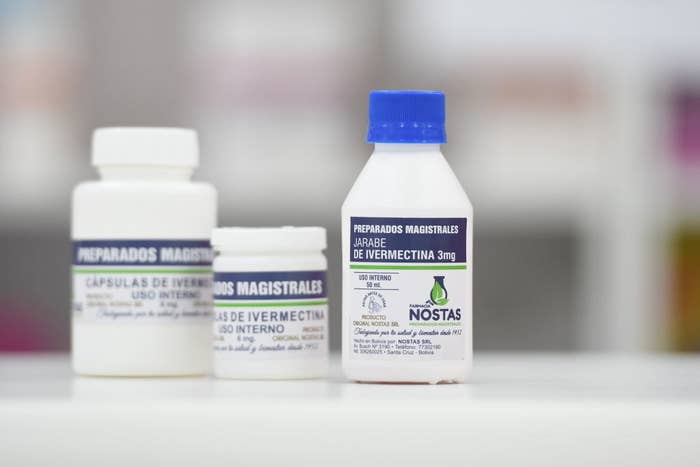
ーー現段階で、イベルメクチンについて「確か」と言えることを教えてください。
まずは、イベルメクチンが新型コロナウイルスに効くのかどうか、というところですが、人体ではなく細胞を使用した実験ではウイルスが増殖することを抑制する効果はあったと報告されています。
ただし、これまで寄生虫への薬として承認されている用量では、効果を発揮する濃度に達しません。アメリカではこれまで使用されている数十倍程度の用量が必要であろうと指摘されています。
つまり、ウイルスそのものへの効果はあるけれども、それが体内で効果を発揮できるかどうかは実際に使ってみた上で検証する必要があります。
既にいくつか臨床研究の結果が報告されていて、その他にもいくつかの臨床研究が現在実施されていますが、現時点で、質の高い臨床研究とその数が十分ではないと評価されています。
つまり、イベルメクチンが新型コロナに対して安全で有効性の高い治療薬である、ということを証明するエビデンス(繰り返し科学的に証明された根拠、検証結果)がまだ不足している状況であると理解しています。
ーー世界各国では、このイベルメクチンについて、どのような対応をしているのでしょうか?
3月8日に米・FDAが新型コロナの治療と予防にイベルメクチンを使用しないよう警鐘を鳴らし、3月22日には欧州・EMAが「臨床試験以外での新型コロナ予防・治療を目的としたイベルメクチンの使用を控えるべき」という勧告を出しました。
更に、3月31日にWHOも同様に、有効性のエビデンスは決定的ではないとし、診療のガイドラインを更新し、同様の推奨を行っています。
現時点では、欧米の規制当局とWHO共にイベルメクチンの有効性と安全性を評価するために臨床試験で用いる場合を除き、治療や予防として使うことは推奨しないと明確にメッセージを発しています。
このような勧告が出ているからイベルメクチンは新型コロナに無効、ということではありません。ですが、「イベルメクチンは新型コロナに有効だ」という確かな結論を現時点で出すことはできていないということです。
医薬品というものは使い方や量によっては毒にもなるものです。身体に作用するときには良いことと悪いことの、両方を想定する必要があります。
そのため、評価方法の質が高い研究での使用データを積み上げて、「このような条件の患者さんにどのように使うことでこういったベネフィット(利益)とリスクがある」との評価が、明らかになった段階で広く使用されるべきだろうと考えます。
医薬品の承認が得られるまでのプロセスとしては、臨床研究で倫理的な配慮と問題が生じた時の体制を確立した上で、その医薬品を多くの人に使ったときの結果が評価されることが必要です。
その上で、科学的妥当性をもって「良いことの方がたくさん起こる」というコンセンサスを得られた医薬品が、製薬会社の申請に基づき、各国の規制当局から承認されます。その結果、その薬剤の製造や流通が可能となります。
その評価があやふやなままに多くの人が使用すれば、一時は新型コロナ治療薬として注目された「ヒドロキシクロロキン」のように、後からあまり効果がないとわかり、むしろ循環器系への副作用が懸念されるということが起こり得ます。
イベルメクチンについては良い効果が多いのか、悪い効果が多いのか、まだ十分に確かではありませんので、「あまり効果がなかった」「むしろ副作用の方が強かった」ということもあるかもしれません。
承認がない段階でも、入手可能な医薬品は、医師の裁量に基づき、十分な説明と理解の上で投薬することができますが、副作用により大きな健康被害が生じても、医学的な裏付けが十分ではなく、承認のない使用法による副作用に対しての被害救済制度は原則として適用されません。
倫理的な配慮がされ、健康問題が生じた際の支援体制が確保された臨床研究で、評価目的に使用する場合を除いて、現時点では新型コロナウイルス感染症の治療にイベルメクチンは使用すべきではないと欧米やWHOは示しています。
「実際に患者に使った際の有効性を証明する研究は十分にはない」
ーー北里大学の大村智記念研究所感染制御研究センターの花木秀明氏は、「予防に89%、早期治療に82%、死亡率にも75%の改善」が見られるとしています。「COVID-19 による入院患者においてイベルメクチン使用は死亡率の低下に関連する」と題した論文をもとにしたこうした評価は、確かなエビデンスに基づくものであると言えるのでしょうか?
まず前提として、結果だけでなくてその研究の方法等の全体を見なければいけません。
一部の研究結果だけにフォーカスしても、その結果を導いた研究の質(参加した患者数やそれぞれの患者の背景、他の薬剤投与など介入の有無、評価方法等の詳細)がわからないためです。
科学的に評価するためには、信頼性(エビデンス)の高さも併せて検討する必要があり、結果だけが一人歩きしないように注意が必要です。
例えば、臨床研究の過程で検証する薬を投与するグループと、投与されていないグループそれぞれに割り付けられた患者さんたちの背景を考えてみましょう。
すでに新型コロナに効くというエビデンスのある「デキサメタゾン」がイベルメクチンの投与されている人に多く使用されているが、イベルメクチンが投与されていないグループにはあまり使用されていないということがあったとします。
このような場合、すでにエビデンスのある薬の効果を見ているのか、それともイベルメクチンの効果を見ているのかがわからなくなってしまいます。
「薬の効果はこのようなものであった」という結果が出たときに、その結果の妥当性を評価するためには、比較したそれぞれのグループの背景にバラつきがないかどうかを確かめる必要があります。
また、併用して使用した薬以外にも、研究結果に影響を与える要因として、重症度にもバラつきがないのかといった患者の背景や、基礎疾患を持っている人が同じくらいいるのか、年齢が高い人だけプラセボ群(検証する薬を投与しない人々)に入っていないかなどが検討されます。
加えて、研究結果の信頼性は、前向き研究*なのか後ろ向き研究*なのか、どのくらいの症例数で検討がされているのか、その薬剤を投与しない「対称群」を置いているのか、患者や効果を評価する医師がどの薬剤を投与されているのかわからない状態(盲検)であるかどうかなど、研究デザインによっても異なります。
※前向き研究:「観察研究」や薬を投与するグループと偽薬を投与するグループにランダムに分けて行うランダム化比較試験をはじめとする「介入研究」などで追跡調査をし、仮説を検証すること
※後ろ向き研究:すでに病気を患っている患者の診療情報や検査結果、組織のサンプルなどを用いてある事柄についてさかのぼって調べる研究のこと
薬剤の投与や結果の評価のタイミングや方法が適切かどうかも医薬品を評価するのに大切な要素です。

また余談ですが、研究の質は、信頼性以外の結果そのものに影響を及ぼすこともあります。
一例として、新型コロナ治療薬として既に承認されている「レムデシビル」の臨床試験を考えてみましょう。
国立国際医療研究センターでも実施された国際的なランダム化比較試験では、薬剤が投与されるタイミングや重症度、病気の状態、併用して投与されている薬の有無などの患者背景から、評価の実施タイミングや内容まで詳細を揃えて評価した結果、有症状期間の短縮などの有効性が見られました。
一方で、WHOが実施した複数の薬剤を同時に評価する(特定の薬剤の評価のために調整がされていない)方法でのランダム化比較試験の評価では、患者数は多いですが、有効性は見出すことができませんでした。
とても丁寧な研究をすれば効果が確認できますが、背景などあらゆる条件を揃えないと別の因子に引っ張られて効果がはっきりと見えてこないということもあり得るものです。
さらに、研究結果の報告内容を第三者の目から評価するための場が査読と呼ばれるプロセスです。
新型コロナの場合、新興感染症であったこともあり、結果を早く世に知らしめたほうが良い、早く次の研究へつなげるべきだということで、査読を経ていない論文(プレプリント)が平時よりも重要視されている部分があるとは思います。そのため、その研究結果が新しく、まだ査読を経ていない場合もあります。
すべての研究が不確定要素を排除することはできないので、評価方法を工夫したり、どのような評価の限界が研究結果にあるのか報告に記載したりすることが求められます。イベルメクチンに関する報告については、比較的小規模であり、様々な評価に影響を与える要素が排除できていない点が、質の高い研究に基づいた評価が不足しているとされる理由であるように思います。
これらの理由から、正しい評価にはできるだけ質の高い研究を実施する必要がありますが、これをやるのも簡単ではありません。大規模なランダム化比較試験を実施するには、時間と労力と費用の観点で非常に大きな負担が生じます。
実社会における別の観点では、製薬会社がその薬を新型コロナ治療薬として販売したいと考えているのかどうか、その薬を新型コロナに積極的に使うべきと考えているのかどうかも、医薬品の承認に影響します。
開発のために医薬品の有効性や安全性のデータを取るための臨床研究には、様々な投資が必要となります。国の薬事承認制度では、原則、製薬会社からの申請に基づくため、医薬品を広く使えるようにできるかどうかは、その医薬品を開発する企業の戦略に依存するものでもあります。
イベルメクチンは、既に低所得国を中心に寄生虫症に対して広く使用されている薬剤であり、非常に安価な薬剤です。この利用しやすさも、イベルメクチンに対する期待と企業の開発意欲に影響を与えている可能性があります。加えて、イベルメクチンは開発には、2015年にノーベル生理学医学賞を受賞されている大村先生など、日本が深く関わっているということも注目や期待を集める要因となっているかもしれません。
こうした様々な要素が複雑に組み合わさって、現在のような議論が生じていると考えられます。
まとめると、承認に必要とされる有効性を確認するためには、質の高い臨床試験が必要となり、そうした臨床試験を行うためには、時間と労力と費用が必要となります。また、承認を申請する主体は、国や研究者ではなく、その薬を製造して販売する製薬会社であることも留意しておくべきでしょう。
繰り返しになりますが、現時点では、イベルメクチンを実際に患者に使った際の有効性及び安全性を証明する質の高い研究は十分であるとは評価されていません。
質の高い臨床研究による有効性を積み上げた上で、承認を経て、広く使用されるべきであると考えます。
イベルメクチンばかりに注目するよりも…

ーーイベルメクチンの「特例承認」を求める声も一部でありますが、どう思われますか?
日本の医薬品の規制は欧米同様に厳しく、基本的には日本人へ使用した臨床データがなければ承認されません。
しかし、
(1)生命及び健康に重大な影響を与える疾病の蔓延の拡大防止のため、緊急に使用される必要がある場合であり、かつ、当該医薬品の使用以外に適当な方法がないこと
(2)その用途に関して、日本と同等の水準にある承認制度を持つ国において、製造販売が承認されていること
この2点を満たす場合には、製薬企業からの申請に基づき、通常時よりも限られたデータでの特例承認が可能となります。
現在、新型コロナウイルス感染症に関して「日本と同等の水準の承認制度を持つ国」として認められているのはイギリス、フランス、ドイツ、カナダ、アメリカの5つの国です。
つまり、日本が世界に先駆けて特例承認をする、といったことは仕組みとして難しく、該当する5つの国のどこかで既に承認され、販売・使用されているものでなければ、特例承認することもできないということにも注意が必要です。
適切な評価に基づいて、確かな効果が確認されれば広く使われる必要があると認められます。その過程は、政治の問題とは独立して、科学的根拠に基づき判断されることが重要です。
そうでないと、誤った評価に基づき、医薬品が流通することで、承認制度や医薬品自体の信頼性が損なわれてしまうリスクが生じます。あくまで冷静かつ客観的に対処するのがよいでしょう。
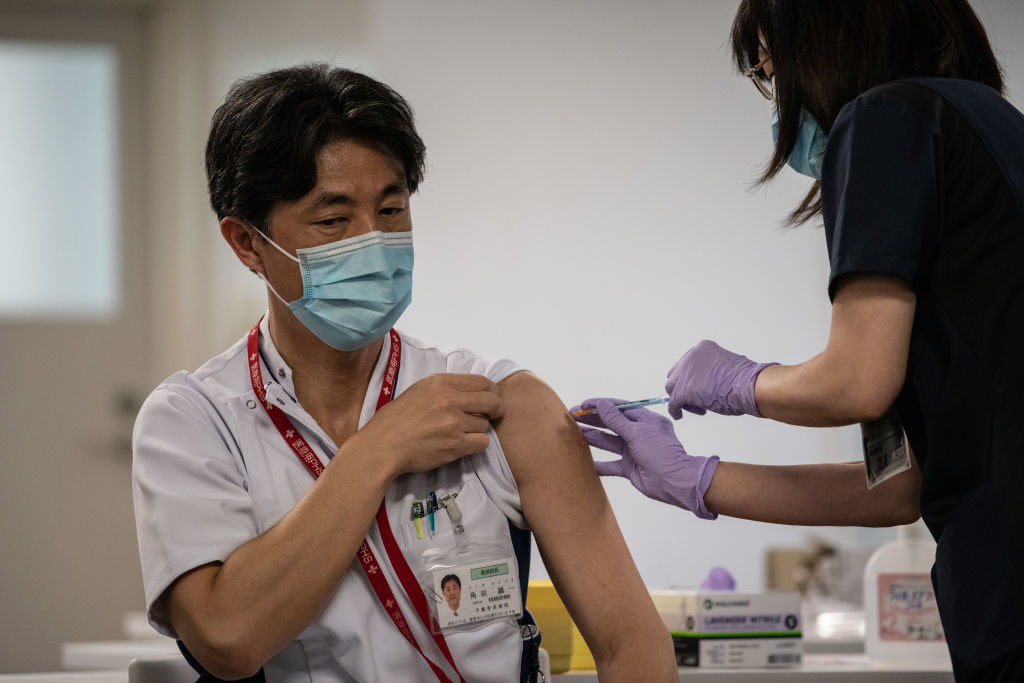
合わせて理解していただきたいのは、現在すでにデキサメタゾンなど有効性が確認されている医薬品が利用可能であり、発症予防効果や重症化予防効果が十分に確認されている新型コロナワクチンの予防接種が始まっているということです。
イベルメクチンの今後の評価も大切ですが、既にエビデンスのある治療薬を正しく使用し、予防のためのワクチンをできるだけ早く、多くの人に接種してもらうことが、社会全体でみたこの新型コロナウイルス感染症対策の要であると思います。
もちろん、これらに加えてイベルメクチンの効果が適切な方法で確認されることを期待しますし、正しい過程を経て、広く使用ができるようになれば、感染対策の大きな助けになるだろうと思います。
ここでお伝えしたいことは、医薬品の新たな使用方法が、本当に有効性及び安全性に問題がないのかをしっかり科学的に評価するプロセスが大切であるという話です。
UPDATE
北里大学の大村智記念研究所感染制御研究センターの花木秀明氏について、「花木秀明医師」と記載していました。花木氏は医師ではありません。訂正いたします。


